Giải khoa học tự nhiên 7 Bài 2: Nguyên tử
Giải khoa học tự nhiên 7 Bài 2: Nguyên tử
Giải khoa học tự nhiên 7 Bài 2: Nguyên tử Sử dụng như tài liệu tham khảo để hiểu rõ hơn, củng cố kiến thức.Mời quý độc giả tham khảo
I. Mở đầu trang 14 Bài 2 KHTN 7
Từ những vật thể đơn giản như cây bút, quyển vở, chai nước cho đến những công trình nổi tiếng như tháp Eiffel,… đều được tạo nên từ chất. Mỗi chất lại được tạo nên từ những hạt vô cùng nhỏ. Những hạt đó là gì?
Hướng dẫn giải
Mỗi chất lại được tạo nên từ những hạt vô cùng nhỏ. Những hạt đó là nguyên tử.
Nguyên tử có kích thước vô cùng nhỏ, tạo nên các chất.
II. Thảo luận
Câu 1 trang 14 Khoa học tự nhiên 7 CTST
Những đối tượng nào trong Hình 2.1 ta có thể quan sát bằng mắt thường? Bằng kính lúp? Bằng kính hiển vi?

Hướng dẫn giải
Đối tượng có thể quan sát bằng mắt thường: Ruột bút chì
Đối tượng quan sát bằng kính lúp: Hạt bụi trong không khí
Đối tượng quan sát bằng kính hiển vi: Tế bào máu, Vi khuẩn
Câu 2 trang 14 Khoa học tự nhiên 7 CTST
Quan sát Hình 2.2, em hãy cho biết khí oxygen, sắt, than chì có đặc điểm chung gì về cấu tạo?

Hướng dẫn giải
Quan sát Hình 2.2, ta có thể thấy khí oxygen, sắt, than chì được cấu tạo từ những quả cầu liên kết với nhau
Câu 3 trang 15 Khoa học tự nhiên 7 CTST
Theo Rutherford – Bohr, nguyên tử có cấu tạo như thế nào?
Hướng dẫn giải
Nguyên tử gồm: hạt nhân ở bên trong và vỏ
+ Vỏ nguyên tử:
Gồm các electron (e) mang điện tích âm được sắp xếp thành từng lớp và chuyển động xung quanh hạt nhân
+ Hạt nhân nguyên tử: Chứa các hạt proton (p) mang điện tích dương
Mỗi proton mang một đơn vị điện tích dương, quy ước là +1.
Câu 4 trang 15 Khoa học tự nhiên 7 CTST
Quan sát Hình 2.5, hãy cho biết nguyên tử nitrogen và potassium có bao nhiêu:
a) Điện tích hạt nhân nguyên tử?
b) Lớp electron?
c) Electron trên mỗi lớp?

Hướng dẫn giải
Nguyên tử nitrogen:
- Điện tích hạt nhân: +7
- Lớp electron: 2 lớp
- Số electron trên mỗi lớp: Lớp thứ 1 có 2 electron, lớp thứ 2 có 5 electron
Nguyên tử potassium:
- Điện tích hạt nhân: +19
- Lớp electron: 4 lớp
- Số electron: Lớp thứ 1 có 2 electron, lớp thứ 2 có 8 electron, lớp thứ 3 có 8 electron, lớp thứ 4 có 1 electron
Câu 5 trang 16 Khoa học tự nhiên 7 CTST
Tại sao nguyên tử trung hoà về điện?
Hướng dẫn giải
Trong mỗi nguyên tử, số hạt proton và electron luôn bằng nhau, chúng có trị số điện tích bằng nhau nhưng trái dấu => Điện tích nguyên tử = 0
Do đó nguyên tử trung hòa về điện
Câu 6 trang 17 Khoa học tự nhiên 7 CTST
Vì sao người ta thường dùng amu làm đơn vị khối lượng nguyên tử?
Hướng dẫn giải
Chỉ với 1 gam chất bất kì đã chứa tới hàng tỉ tỉ nguyên tử
Ví dụ: Trong 1 gam carbon có chứa khoảng 50.1021 nguyên tử carbon
Như vậy 1 nguyên tử carbon có khối lượng
1 nguyên tử có khối lượng 1,9926 .10-23 gam
Khối lượng nguyên tử rất nhỏ nên để biểu thị khối lượng nguyên tử người ta sử dụng đơn vị khối lượng nguyên tử là amu = 1,6605.10-24
II. Luyện tập
Luyện tập Trang 16 Khoa học tự nhiên 7 CTST
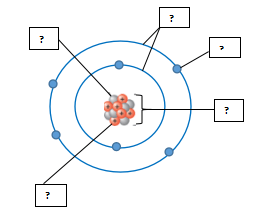
1. Cho biết các thành phần cấu tạo nên nguyên tử trong hình minh hoạ sau:
2. Quan sát Hình 2.6, hãy hoàn thành bảng sau:
| Số đơn vị điện tích hạt nhân | Số proton | Số electron trong nguyên tử | Số electron ở lớp ngoài cùng |
| ? | ? | ? | ? |
Để lớp electron ngoài cùng của nguyên tử oxygen có đủ số electron tối đa thì cần thêm bao nhiêu electron nữa?

Hướng dẫn giải
1. Thành phần cấu tạo nên nguyên tử trong hình minh hoạ sau

2.
Số đơn vị điện tích hạt nhân = số electron = số proton
Nguyên tử oxygen có 8 electron
=> Số đơn vị điện tích hạt nhân = số proton = số electron = 8
| Số đơn vị điện tích hạt nhân | Số proton | Số electron trong nguyên tử | Số electron ở lớp ngoài cùng |
| 8 | 8 | 8 | 2 |
Lớp thứ 2 có tối đa 8 electron, mà lớp thứ 2 của oxygen có 6 electron
=> Để lớp electron ngoài cùng của nguyên tử oxygen có đủ số electron tối đa thì cần thêm 2 electron nữa
Luyện tập Trang 17 Khoa học tự nhiên 7 CTST
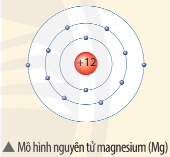
Quan sát mô hình dưới đây và cho biết số proton, số electron và xác định khối lượng nguyên tử magnesium (biết số neutron bằng 12).
Hướng dẫn giải
Mô hình nguyên tử magnesium có đơn vị điện tích hạt nhân = 12
=> Số electron = số proton = số đơn vị điện tích hạt nhân = 12
Khối lượng nguyên tử magnesium = số proton x 1 amu + số neutron x 1 amu = 12 x 1 amu + 12 x 1 amu = 12 amu
III. Câu hỏi Bài tâp
Bài 1 trang 17 Khoa học tự nhiên 7 CTST
Em hãy điền vào chỗ trống các từ, cụm từ thích hợp sau để được câu hoàn chỉnh:
| chuyển động | các electron | hạt nhân | điện tích dương | trung hòa về điện |
| vỏ nguyên tử | điện tích âm | vô cùng nhỏ | sắp xếp |
Nguyên tử là hạt…(1) và (2)… Theo Rutherford – Bohr, nguyên tử có cấu tạo gồm 2 phần là (3)…(mang (4)…) và (5)… tạo bởi (6)… (mang (7)…)
Trong nguyên tử, các electron (8)…xung quanh hạt nhân và (9)… thành từng lớp.
Hướng dẫn giải
Nguyên tử là hạt vô cùng nhỏ và trung hòa về điện. Theo Rutherford – Bohr, nguyên tử có cấu tạo gồm 2 phần là hạt nhân (mang điện tích dương) và vỏ nguyên tử tạo bởi các electron (mang điện tích âm)
Trong nguyên tử, các electron chuyển động xung quanh hạt nhân và sắp xếp thành từng lớp
Bài 2 trang 17 Khoa học tự nhiên 7 CTST
Vì sao nói khối lượng hạt nhân được coi là khối lượng nguyên tử
Hướng dẫn giải
Ta có:
+ Khối lượng 1 proton = 1 neutron = 1amu
+ Khối lượng 1 electron = 0,00055 amu
Suy ra khối lượng electron nhỏ hơn rất nhiều so với khối lượng proton và neutron
Vậy có thể bỏ qua khối lượng của electron hay khối lượng hạt nhân nguyên tử có thể coi là khối lượng của nguyên tử.
