Khoa học tự nhiên 9 bài 23:Alkane
Khoa học tự nhiên 9 bài 23:Alkane
Giải khoa học tự nhiên 9 bài 23 có đáp án chi tiết cho từng bài tập trong sách Kết nối tri thức mới. Hi vọng sẽ là tài liệu giúp các em tham khảo và đối chiếu với lời giải của mình để hoàn thành tốt bài tập.
Khoa học tự nhiên 9 bài 23 trang 107
Mở đầu trang 107 Bài 23 Khoa học tự nhiên 9
Khí mỏ dầu hóa lỏng (dùng cho bật lửa và bếp gas), xăng hay dầu (dùng cho xe máy, ô tô, máy bay, …) đều có thành phần chính là alkane. Dựa trên những tính chất gì mà các alkane được sử dụng làm nhiên liệu? Alkane còn có những ứng dụng gì khác?
Trả lời:
Phản ứng cháy của alkane toả nhiệt mạnh, vì vậy alkane được sử dụng làm nhiên liệu trong cuộc sống và sản xuất.
Ngoài được sử dụng làm nhiên liệu, alkane còn được sử dụng làm nguyên liệu trong tổng hợp hữu cơ.
I. Khái niệm hydrocarbon, alkane
Hoạt động trang 107 Khoa học tự nhiên 9
Tìm hiểu về các hydrocarbon thông dụng
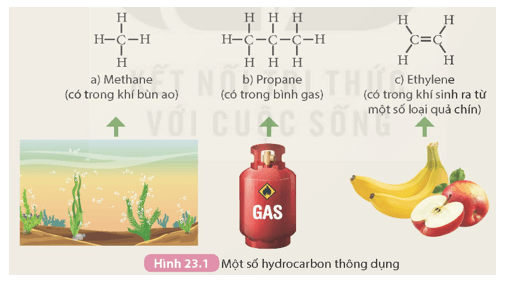
Quan sát Hình 23.1 và thực hiện các yêu cầu sau:
1. Nhận xét đặc điểm chung về thành phần nguyên tố của ba chất trên.
2. So sánh đặc điểm cấu tạo (loại liên kết cộng hóa trị) giữa các nguyên tử trong phân tử của ba chất trên.
Trả lời:
1. Ba chất trên chỉ chứa hai nguyên tố là carbon (C) và hydrogen (H).
2.
| Liên kết giữa C và H | Liên kết giữa C và C | |
| a) Methane | Liên kết đơn | Không có |
| b) Propane | Liên kết đơn | Liên kết đơn |
| c) Ethylene | Liên kết đơn | Liên kết đôi |
Khoa học tự nhiên 9 bài 23 trang 108
Câu hỏi 1 trang 108 Khoa học tự nhiên 9
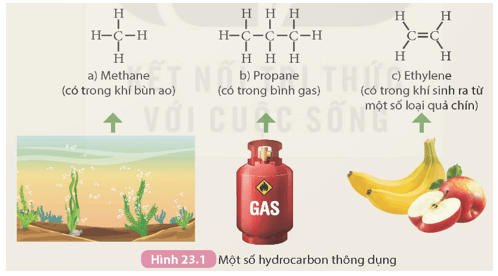
Quan sát Hình 23.1 và cho biết hợp chất nào không thuộc loại alkane. Giải thích.
Trả lời:
Ethylene là hợp chất không thuộc loại alkane thì trong phân tử chứa liên kết đôi.
Câu hỏi 2 trang 108 Khoa học tự nhiên 9
Xét các chất:
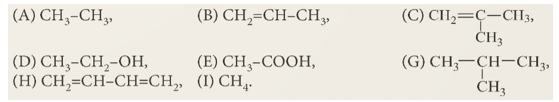
Trong các chất trên, chất nào là hydrocarbon, chất nào là alkane? Giải thích.
Trả lời:
Ta có:
– Hydrocarbon là loại hợp chất hữu cơ mà thành phần phân tử chỉ chứa các nguyên tố carbon và hydrogen.
– Alkane là những hydrocarbon mạch hở, phân tử chỉ chứa các liên kết đơn.
Nên:
– Hydrocarbon gồm: A, B, C, G, H, I
– Alkane gồm: A, G, I
II. Cấu tạo phân tử và danh pháp của alkane
Hoạt động trang 108 Khoa học tự nhiên 9
Đọc thông tin trong Bảng 23.1 và thực hiện các yêu cầu sau:
1. Trong công thức phân tử của alkane, khi tăng thêm một nguyên tử carbon thì số nguyên tử hydrogen tăng thêm là bao nhiêu?
2. Hãy cho biết tên gọi của các alkane trong Bảng 23.1 có đặc điểm gì giống nhau và khác nhau.
Trả lời:
1. Trong công thức phân tử của alkane, khi tăng thêm một nguyên tử carbon thì số nguyên tử hydrogen tăng thêm là hai.
2.Giống nhau: cuối tên gọi đều có cụm ane.
Khác nhau: các alkane có số carbon khác nhau nên có tên gọi khác nhau.
III. Phản ứng cháy của Alkane
Khoa học tự nhiên 9 bài 23 trang 109
Hoạt động trang 109 Khoa học tự nhiên 9
Thí nghiệm: Tìm hiểu về phản ứng cháy của butane
Chuẩn bị: Bật lửa gas (chứa butane) loại dài (loại dùng để mồi lửa bếp gas, bếp cồn); bình tam giác bằng thuỷ tinh chịu nhiệt, sạch và khô, có nút; ống nghiệm đựng dung dịch nước vôi trong.
Tiến hành:
– Đưa đầu bật lửa vào miệng bình tam giác úp ngược, đánh lửa và giữ lửa cháy cho tới khi thấy thành bình tam giác mờ đi thì dừng lại (Hình 23.2).

– Quay xuôi bình tam giác lại và đổ nước vôi trong vào. Sau đó, đậy bình tam giác bằng nút và lắc đều.
Thực hiện yêu cầu sau:
1. Nhận xét hiện tượng bên trong thành bình tam giác sau khi đánh lửa bật lửa gas để đốt cháy butane. Dự đoán sản phẩm tạo thành.
2. Quan sát hiện tượng xảy ra trong bình tam giác sau khi cho nước vôi trong vào bình và dự đoán sản phẩm tạo thành.
Trả lời:
1. Hiện tượng bên trong thành bình tam giác sau khi đánh bật lửa gas để đốt cháy butane là dần dần thấy bình tam giác mờ đi. Sản phẩm tạo thành là CO2 và H2O.
2. Hiện tượng xảy ra trong bình tam giác sau khi cho nước vôi trong vào bình là khí CO2 làm vẩn đục nước vôi trong. Sản phẩm tạo thành là CaCO3 và H2O.
Câu hỏi 1 trang 109 Khoa học tự nhiên 9
a) Viết phương trình hóa học biểu diễn phản ứng cháy của methane và ethane.
b) Dùng công thức chung của alkane, viết phương trình hóa học tổng quát của phản ứng đốt cháy hoàn toàn alkane tạo thành sản phẩm là carbon dioxide và nước.
Trả lời:
a) $CH4+2O2 \overset{to}{\rightarrow} CO2 +2H2O$
$2C2H6+7O2 \overset{to}{\rightarrow} 4CO2+6H2O$
b)
$CnH_{2n+2}$ +$\frac{3n+1}{2}$ $O2\overset{to}{\rightarrow}nCO2+(n+1)H2O$
Câu hỏi 2 trang 109 Khoa học tự nhiên 9
Giả thiết rằng gas trong bình gas là một hỗn hợp propane và butane có tỉ lệ thể tích 1:1. Tính nhiệt lượng sinh ra khi đốt cháy 1 kg loại gas này. Biết rằng nhiệt lượng tương ứng sinh ra khi đốt cháy 1 mol mỗi chất propane và butane lần lượt là 2 220kJ và 2 878 kJ.
Trả lời:
Ta có hỗn hợp propane và butane có tỉ lệ thể tích 1:1 nên số mol của propane và butane trong hỗn hợp bằng nhau.
Giả sử: npropane= nbutane= x (mol)
Khi đốt cháy 1 kg loại gas, ta có:
44x + 58x = 1000
→ x ≈ 9,8 mol
Nhiệt lượng sinh ra khi đốt cháy 1 kg loại gas này là:
Q = 9,8.2220 + 9,8.2878 = 49960,4 kJ
IV. Ứng dụng làm nhiên liệu của Alkane
Khoa học tự nhiên 9 bài 23 trang 110
Câu hỏi 1 trang 110 Khoa học tự nhiên 9
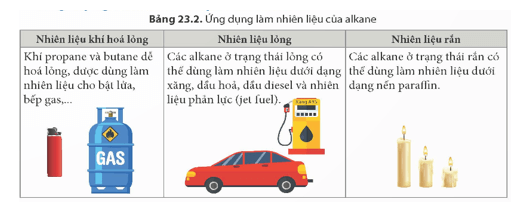
Đọc thông tin trong Bảng 23.2 và trình bày các ứng dụng chủ yếu của alkane.
Trả lời:
Các ứng dụng chủ yếu của alkane:
– Khí propane và butane dễ hóa lỏng, được dùng làm nhiên liệu cho bật lửa, bếp gas, …
– Các alkane ở trạng thái lỏng có thể dùng làm nhiên liệu dưới dạng xăng, dầu hỏa, dầu diesel và nhiên liệu phản lực.
– Các alkane ở trạng thái rắn có thể dùng làm nhiên liệu dưới dạng nến paraffin.
Câu hỏi 2 trang 110 Khoa học tự nhiên 9
Bảng dưới đây cho biết nhiệt lượng tỏa ra khi đốt cháy hoàn toàn 1 mol alkane.
| Alkane | Công thức phân tử | Khối lượng mol phân tử (gam/mol) | Nhiệt lượng (kJ/mol) |
| Methane | CH4 | 16 | 891 |
| Ethane | C2H6 | 30 | 1 561 |
| Propane | C3H8 | 44 | 2 220 |
| Butane | C4H10 | 58 | 2 878 |
a) Tính nhiệt lượng tỏa ra khi đốt cháy hoàn toàn 1 gam mỗi alkane trong bảng trên.
b) Đốt cháy 1 gam alkane nào trong số các alkane ở trên sẽ tỏa ra nhiều nhiệt lượng nhất?
Trả lời:
a)
| Alkane | Số mol (mol) | Nhiệt lượng tỏa ra (kJ) |
| Methane | $\frac{1}{16}$ =0,0625 | 0,0625.891 = 55,6875 |
| Ethane | $\frac{1}{30}$≈0,0333 | 0,0333.1561 = 51,98 |
| Propane | $\frac{1}{44}$≈0,0227 | 0,0227.2220 = 50,39 |
| Butane | $\frac{1}{58}$≈0,0172 | 0,0172.2878 = 49,50 |
b) Khi đốt cháy 1 gam alkane trong số các alkane ở trên thì methane sẽ tỏa ra nhiệt lượng nhiều nhất.
